ģÆč§░▒č§╗»(Anammox)╣ż╦ćū„×ķę╗ĒŚą┬ą═Īó╣Ø─▄Ą─╔·╬’├ōĄ¬╝╝ągŻ¼╩▄ĄĮ┴╦蹊┐š▀Ą─ÅVĘ║ĻPūóŻ¼ę“Ųõ─▄į┌ģÆ觌l╝■Ž┬Ż¼└¹ė├░▒Ą¬Īóü厧Ą¬ū„×ķļŖūė╣®¾w║═ļŖūė╩▄¾wŻ¼īóČ■š▀═¼Ģr▐DōQ×ķĄ¬ÜŌČ°Å─Ę┤款wŽĄųą╚ź│²ĪŻ╚╗Č°įō▀^│╠└Ēšō╔ŽĢ■ī¦ų┬11%Ą─Ž§╦ß¹}Ą¬╔·│╔Ż¼×ķ┐饬╚ź│²┬╩Ą─╠ßĖ▀ĦüĒ╠¶æĪŻŪęģÆč§░▒č§╗»Š·(AnAOB)▒Čį÷ĢrķgķLŻ¼Š▀ėą╔·╬’┘|ęū┴„╩¦ĪóŁhŠ│├¶ĖąČ╚Ė▀Ą─╠ž³cŻ¼ęū╩▄ĄĮĖ▀ØŌČ╚Ą¬╦žÄ¦üĒĄ─ęųųŲū„ė├Ż¼Å─Č°ė░Ēæ¾wŽĄĄ─Ą¬╚ź│²ą¦┬╩║═ĘĆČ©ąįĪŻ
×ķ┴╦Ė─╔Ų─┐Ū░AnammoxĘ┤款wŽĄ┤µį┌Ą─▓╗└¹Śl╝■Ż¼═Č╝ė╔·╬’╠┐│╔×ķ┴╦ę╗ĘNÅVĘ║▓╔ė├Ą─ĘĮ╩ĮĪŻ╔·╬’╠┐┐╔ęį═©▀^│õ«öļŖūėĮķī¦¾w┤┘▀MAnammox¾wŽĄųą└█ĘeŽ§Ą¬Ą─▀ĆįŁÅ─Č°╠ß╔²┐饬╚ź│²ą¦╣¹Ż¼═¼Ģrę▓─▄═©▀^┤┘▀M╝ÜŠ·░¹═ŌŠ█║Ž╬’(EPS)Ą─Ęų├┌Īóį÷ÅŖ╣”─▄╗∙ę“Ą─▒Ē▀_ęįŠÅĮŌĘ┤款wŽĄĖ▀Ą¬žō║╔ī¦ų┬Ą─╬ó╔·╬’ęųųŲĪŻLIĄ╚蹊┐Ą├│÷į┌100mgNĪżL−1Ą─AnammoxĘ┤款wŽĄųąŻ¼╔·╬’╠┐Ą─═Č╝ė╩╣Ž§Ą¬▀ĆįŁ╦┘┬╩╠ß╔²┴╦2.2▒ČŻ¼Ūę╔·╬’╠┐╠ß╔²┴╦AnAOB║═Ę┤Ž§╗»Š·(DNB)Ą╚╣”─▄╝ÜŠ·Ą─žSČ╚Ż╗CHENĄ╚蹊┐Ą├│÷Anammox╗Ņąįį┌┐饬┘|┴┐ØŌČ╚┤¾ė┌250mgNĪżL−1ĢrųØuŽ┬ĮĄŻ¼╔·╬’╠┐╩╣╔ŽŽ▐╠ßĖ▀ų┴300mgNĪżL−1Ż╗Č°LIĄ╚蹊┐▒Ē├„┐饬┘|┴┐ØŌČ╚į┌440mgNĪżL−1ĢrŻ¼¾wŽĄŠ▀ėąĖ³Ė▀Ą─╬ó╔·╬’EPSĘų├┌┘|┴┐ØŌČ╚ęį╝░Ė³┤¾Ą─AnAOBŽÓī”žSČ╚ĪŻę“┤╦Ż¼╔·╬’╠┐į┌▓╗═¼Ą¬žō║╔Ž┬ī”AnammoxĘ┤款wŽĄĄ─ė░Ēæą¦╣¹▓Ņ«É▌^┤¾ĪŻ─┐Ū░蹊┐ČÓ×ķå╬ę╗žō║╔Ž┬╔·╬’╠┐ī”Anammox¾wŽĄĄ─ė░ĒæŻ¼Č°▓╗═¼Ą¬žō║╔Ž┬╔·╬’╠┐Įķī¦AnammoxĘ┤款wŽĄ├ōĄ¬╠žš„Ą─▓Ņ«É┼cū„ė├ÖC└Ē╚į▓╗├„┤_Ż¼═¼Ģr▓╗═¼žō║╔ė░ĒæŽ┬╔·╬’╠┐ī”╬ó╔·╬’╚║┬õč▌╠µ║═┤·ųx═ŠÅĮĄ─ūā╗»ęÄ┬╔╚įėą┤²▀Mę╗▓Į╠ĮŠ┐ĪŻ
ę“┤╦Ż¼▒ŠčąŠ┐═©▀^▀Mąą┼·┤╬īŹ“×┐╝▓ņ┴╦3ĘNĄ¬žō║╔Śl╝■Ž┬(┐饬×ķ100Īó300Īó500mgNĪżL−1)╔·╬’╠┐ÅŖ╗»Anammox¾wŽĄ├ōĄ¬ąį─▄Ą─╠žš„Ż¼ĮY║ŽĄ¬▐D╗»▀^│╠┼c╔·╬’╠┐▒Ēš„ĪóEPSĪó╬ó╔·╬’Ęų▓╝Īó╚║┬õĮYśŗęį╝░╣”─▄ŅA£yĄ─Ęų╬÷Ż¼╠Įėæ┴╦╔·╬’╠┐ÅŖ╗»▓╗═¼Ą¬žō║╔Ę┤款wŽĄ├ōĄ¬▀^│╠Ą─▓Ņ«É┼cį÷ą¦ÖC└ĒĪŻ
1Īó▓─┴Ž┼cĘĮĘ©
1.1 ╠┐▓─┴ŽųŲéõ┼c└Ē╗»ąį┘|£yČ©
▒ŠčąŠ┐╔·╬’╠┐įŁ┴Ž▓╔ė├╠O╣¹─Š─Šą╝ĪŻīó─Šą╝ų├ė┌±RĖźĀtā╚Ż¼ė┌300ĪµŚl╝■Ž┬¤ßĮŌ2h║¾└õģsų┴╩ę£žŻ¼ę└┤╬═©▀^18─┐┼c35─┐║YŠW▀Mąą║YĘųŻ¼▀x╚Ī┴ŻÅĮ0.5~1mm╔·╬’╠┐Ė╔į’├▄ĘŌ▒Ż┤µĪŻ
═©▀^ĖĄ└’╚~ūāōQ╝t═Ō╣ŌūVāx(NicoletiS20Ż¼├└ć°┘É─¼’w╩└Ā¢┐Ų╝╝╣½╦Š)£yČ©╔·╬’╠┐▒Ē├µ╣┘─▄łFŻ╗ł÷░l╔õÆ▀├ĶļŖūė’@╬óńR(Quanta650FŻ¼├└ć°FEI╣½╦Š)┼─öz╔·╬’╠┐ą╬├▓ĮYśŗŻ╗īó║µĖ╔║¾Ą─╔·╬’╠┐čą─ź│╔Ę█─®(▀^200─┐║Y)Ż¼╚Ī50mg╔·╬’╠┐Ę█─®ęį╝░ŽĪßī10▒ČĄ─▌┴Ęė(C10H8O)╚▄ę║ęį1Ī├6Ą─▒╚└²╗ņ║Ž▓ó│¼┬Ģ30minŻ¼╩╣Ųõ│õĘųĮėė|ĪŻīó╗ņ║Ž╚▄ę║Ą╬╝ė100”╠Lė┌▓Ż╠╝ļŖśO╔ŽŻ¼35Īµ║µĖ╔║¾▀Mąą╩╣ė├ļŖ╗»īW╣żū„šŠ(CHI660EŻ¼╔Ž║Ż│Į╚AāxŲ„ėąŽ▐╣½╦Š)┼c╚²ļŖśO¾wŽĄļŖĮŌ│ž(╚▌Ęe100mL)▀MąąčŁŁhĘ³░▓Ę©(CV)£yČ©Ż¼▒Ēš„Ę┤æ¬Ū░║¾╔·╬’╠┐Ą─ļŖ╗»īWąį─▄ūā╗»ĪŻ
1.2 ĘN─Ó╝░įć“׌l╝■įOų├
▒ŠčąŠ┐╩╣ė├ĘN─Ó╚ĪūįīŹ“×╩ęĘĆČ©▀\ąą┼“├øŅw┴Ż╬█─Ó┤▓(expandedgranularsludgebedŻ¼EGSB)Ę┤æ¬Ų„Ż¼▀\ąą£žČ╚×ķ35ĪµŻ¼╦«┴”═Ż┴¶Ģrķg(hydraulicretentiontimeŻ¼HRT)×ķ10hŻ¼╬█─Ó┘|┴┐ØŌČ╚MLSSĪóMLVSSĘųäe×ķ7500Īó4700mgĪżL−1Ż¼Ņw┴Ż╬█─Ó│╩╝t║ų╔½ĪŻįć“×Ū░Ž┤£ņĘN─ÓŻ¼╝ė╚ļ╚źļxūė╦«╗ņ║Ž║¾āAĄ╣╔ŽŪÕę║▓óųžÅ═3┤╬Ż¼ęį╚ź│²Üł┴¶Ą─NH4+ĪóNO2−║═NO3−Ż¼£p╔┘ī”įć“ץ─ė░ĒæĪŻ┼·┤╬įć“׊∙į┌╣żū„¾wĘe×ķ100mLĄ─č¬ŪÕŲ┐ųą▀MąąŻ¼Ę┤款wŽĄųą╬█─Ó┘|┴┐ØŌČ╚MLSSĪóMLVSSĘųäe×ķ1100Īó700mgĪżL−1ĪŻĘŌŲ┐Ū░ė├Ą¬ÜŌ┤ĄÆ▀3minęį╚ź│²č¬ŪÕŲ┐Ēö▓┐č§ÜŌŻ¼▓ó┴ó╝┤ė├Ž─z╚¹║═õX╔w├▄ĘŌĪŻ╦∙ėą┼·┤╬įć“׊∙į┌║Ń£žš±╩ÄŲ„ųą▀MąąŻ¼š±╩Ä╦┘Č╚║═£žČ╚Ęųäe┐žųŲį┌120rĪżmin−1║═35ĪµĪŻ
1.3 ▓╗═¼Ą¬žō║╔├ōĄ¬┼·┤╬īŹ“×
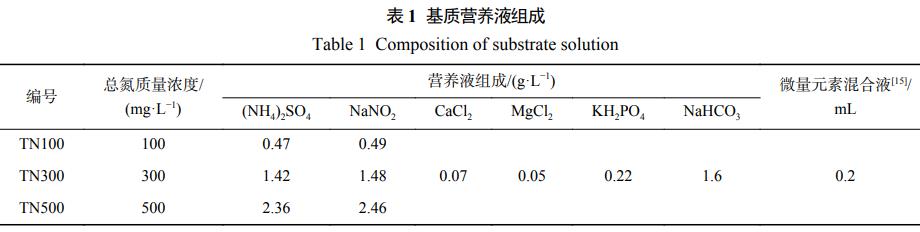
įOų├3ĮM╗∙┘|┘|┴┐ØŌČ╚Ż¼Ęųäe×ķ┐饬100Īó300Īó500mgĪżL−1Ż¼├³├¹×ķTN100ĪóTN300ĪóTN500ĪŻ▓╔ė├╚╦╣ż┼õ╦«Ż¼Ž“┐é╚▌Ęe×ķ120mLĄ─č¬ŪÕŲ┐ųą╝ė╚ļ50mLĀIBę║Ż¼15mLĘN─Óęį╝░35mL╚źļxūė╦«ęį½@Ą├100mLĄ─╣żū„¾wĘeĪŻ╔·╬’╠┐═Č╝ė┴┐×ķ10gĪżL−1ĪŻĀIBę║ĮM│╔ęŖ▒Ē1ĪŻ
1.4 Öz£yĒŚ─┐╝░ĘĮĘ©
1)╦«┘|ųĖś╦£yČ©ĪŻ
╩╣ė├1mL¤oŠ·ßś╣▄╚Ī│÷╦«śė║¾Įø╬ó┐ū▀^×VŲ„(0.45”╠m)▀^×VŻ¼▀^×V║¾Ą─╦«śėė├ė┌Ęų╬÷NH4+ĪóNO2−ĪóNO3−Ą─┘|┴┐ØŌČ╚ĪŻNH4+-N▓╔ė├╝{╩Žįćä®Ęų╣Ō╣ŌČ╚Ę©£yČ©Ż¼NO2−-N▓╔ė├N-(1-▌┴╗∙)-ęęČ■░Ę╣ŌČ╚Ę©£yČ©Ż¼NO3--N▓╔ė├░▒╗∙╗Ū╦ßĘų╣Ō╣ŌČ╚Ę©£yČ©ĪŻ
2)░¹═ŌŠ█║Ž╬’╠ß╚Ī┼c£yČ©ĪŻ
╚Īč¬ŪÕŲ┐ā╚╚½▓┐╬█─Ó╝ė╚ļ50mLļxą─╣▄Ż¼╝ė╝ā╦«ų┴45mLĪŻŅA└õļxą─ÖCų┴4ĪµŻ¼4000r∙min−1ļxą─10minŻ¼╚Ī╔ŽŪÕę║▀^×VĄ├ĄĮSMP(solublemicrobialproduct)Ż╗╝ė╚ļ70ĪµĄ─5ĪļĄ─NaCl╚▄ę║ų┴45mLĪŻ£uą²š±╩Ä1minŻ¼6000r∙min−1ļxą─10min║¾▀^×V╔ŽŪÕę║Ą├ĄĮ╦╔╔óĮY║Žą═EPS(LB-EPS)Ż╗ūŅ║¾īóļxą─╣▄╝ė╚ļ70ĪµĄ─5ĪļĄ─NaCl╚▄ę║ų┴45mLŻ¼▓óį┌70Īµ╦«įĪ30minŻ¼6000r∙min−1ļxą─10min║¾▀^×V╔ŽŪÕę║Ą├ĄĮŠo├▄ĮY║Žą═EPS(TB-EPS)ĪŻ╠ß╚ĪEPS║¾║µĖ╔╬█─ÓŻ¼╩╣ė├±RĖźĀtņč¤²║¾═©▀^▓Ņųžėŗ╦Ń╬ó╔·╬’┘|┴┐(gvss)ĪŻ╠ß╚ĪĄ─3ĘN░¹═ŌŠ█║Ž╬’Ęųäe▓╔ė├▒ĮĘė-┴“╦ßĘ©ĪóFolin-ĘėĘ©£yČ©ČÓ╠Ū(PS)ĪóĄ░░ū┘|(PN)Ą─┘|┴┐ØŌČ╚ĪŻ
3)╚²ŠS¤╔╣Ō╣ŌūV£yČ©ĪŻ
▓╔ė├╚š┴ó¤╔╣ŌĘų╣Ō╣ŌČ╚ėŗ(F-7000Ż¼╚š▒ŠHitachi╣½╦Š)£yČ©EPSĄ─¤╔╣Ō╠žąįŻ¼░l╔õ▓©ķLĘČć·×ķ200~500nmŻ¼╝ż░l▓©ķL×ķ250~550nmŻ¼Æ▀├ĶķgĖ¶5nmŻ¼Æ▀├Ķ╦┘Č╚×ķ12000nmĪżmin−1ĪŻ
1.5 ėŗ╦ŃĘĮĘ©
Ė∙ō■╣½╩Į(1)~(5)ėŗ╦Ń┐饬╚ź│²ą¦┬╩(TNRE)Īó┐饬╚ź│²╦┘┬╩(TNRR)Īó░▒Ą¬╚ź│²╦┘┬╩(NRR░▒Ą¬)Īóü厧Ą¬╚ź│²╦┘┬╩(NRRü厧Ą¬)╝░Ž§Ą¬▀ĆįŁ╦┘┬╩(NRRŽ§Ą¬)ĪŻ

╩ĮųąŻ║Ę┤æ¬Ū░║¾┐饬Ą─┘|┴┐ØŌČ╚ūā╗»Ż¼mgĪżL−1Ż╗Ż║│§╩╝┐饬┘|┴┐ØŌČ╚(░▒Ą¬Īóü厧Ą¬Ī󎧥¬ų«║═)Ż¼mgĪżL−1Ż╗ĪóŻ║Ę┤æ¬Ū░║¾░▒Ą¬Īóü厧Ą¬Ą─┘|┴┐ØŌČ╚ūā╗»Ż¼mgĪżL−1Ż╗Ż║└█ĘeŽ§Ą¬┘|┴┐ØŌČ╚ūŅ┤¾ųĄ┼cĘ┤æ¬ĮY╩°┘|┴┐ØŌČ╚▓ŅŻ¼mgĪżL−1Ż╗Ż║ī”æ¬Ę┤æ¬╣سcĢrķg▓ŅŻ¼hĪŻ1.6╬ó╔·╬’╚║┬õĮYśŗ┼c╣”─▄Ęų╬÷Ę┤æ¬ĮY╩°║¾▀x╚ĪĖ„īŹ“×ī”ššĮM┼c╔·╬’╠┐ĮM╬█─Óśė▒Šę╗╩ĮČ■Ę▌▀Mąą16S╬ó╔·╬’ĘųŅÉ£yą“ĪŻ╩╣ė├E.Z.N.A™Mag-Bind═┴╚└DNAįćä®║ą(M5635-02Ż¼├└ć°OmegaBiotek╣½╦Š)╠ß╚Ī╚║┬õ╗∙ę“ĮMDNAŻ¼╩╣ė├Qubit4.0£y┴┐DNAĄ─┘|┴┐ØŌČ╚Ż¼┤_▒Ż╠ß╚ĪūŃē“Ą─Ė▀┘|┴┐DNAŲ¼Č╬ĪŻį┌╝ÜŠ·16SrRNA╗∙ę“Ą─Ė▀ūāģ^V3©CV4╩╣ė├š²Ž“ę²╬’(341FŻ¼CCTACGGGNGGCWGCAG)║═Ę┤Ž“ę²╬’(805RŻ¼GACTACHVGGGTATCTAATCC)▀MąąPCRöUį÷ĪŻ£yą“═Ļ│╔║¾Ż¼╩╣ė├PEAR╠Ä└Ēfastq╬─╝■╔·│╔å╬¬ÜĄ─fasta║═qual╬─╝■Ż¼═©▀^Usearchī”ŽÓ╦ŲąįĖ▀ė┌97%Ą─OTU▀MąąŠ█ŅÉŻ¼▀xō±žSČ╚ūŅĖ▀Ą─ś╦ėøą“┴ąū„×ķ├┐éĆŠ█ŅÉĄ─┤·▒Ēą“┴ąŻ¼└¹ė├RDPöĄō■Äņī”╝ÜŠ·OTU┤·▒Ēą“┴ą▀MąąĘųŅÉ▓ó▀Mąą╚║┬õČÓśėąįųĖöĄėŗ╦ŃĪŻ└¹ė├PICRUStī”╝ÜŠ·▀Mąą┤·ųx═©┬Ę╣”─▄ŅA£yĘų╬÷ĪŻ
2ĪóĮY╣¹┼cėæšō
2.1 ╔·╬’╠┐ī”▓╗═¼Ą¬žō║╔Ę┤款wŽĄ├ōĄ¬▀^│╠į÷ą¦Ęų╬÷
TN100ĪóTN300ĪóTN500ī”ššĮMūŅĮK┐饬╚ź│²┬╩×ķ86.4%Īó85.1%║═88.2%Ż¼╔·╬’╠┐Ą─═Č╝ė╩╣Ė„ī”ššĮMĄ─╚ź│²┬╩Ęųäe╠ßĖ▀┴╦13.6%Īó4.5%║═1.8%(łD1)Ż¼╝┤╔·╬’╠┐ī”▓╗═¼Ą¬žō║╔Ę┤款wŽĄ┐饬╚ź│²Š∙ėą┤┘▀Mą¦╣¹Ż¼Ūę┤┘▀Mą¦╣¹TN100>TN300>TN500ĪŻ═¼ĢrŻ¼Ę┤æ¬ĮY╩°║¾Ė„īŹ“×ĮMųąĄ─TN100╔·╬’╠┐ĮMŠ▀ėąūŅĖ▀Ą─TNRR(0.103gNĪżL−1Īżd−1)ęį╝░ūŅĖ▀Ą─TNRE(100%)Ż¼šf├„Ą═žō║╔Śl╝■Ž┬╔·╬’╠┐ī”ģÆč§░▒č§╗»¾wŽĄ┐饬╚ź│²Ą─╠ß╔²ą¦╣¹Ė³╝čĪŻļSų°┐饬┘|┴┐ØŌČ╚Ą─£p╔┘Ż¼Ę┤æ¬▀^│╠┐╔äØĘų×ķ┐ņ╦┘Ę┤æ¬ļAČ╬ęį╝░┬²╦┘Ę┤æ¬ļAČ╬ĪŻ3ĘNĄ¬žō║╔Ą─AnammoxĘ┤款wŽĄĘ┤æ¬ļAČ╬ūā╗»╣سcĘųäeį┌12Īó25Īó54hĪŻį┌┐ņ╦┘Ę┤æ¬ļAČ╬ųąŻ¼░▒Ą¬┼cü厧Ą¬│õūŃŻ¼├ōĄ¬▀^│╠ęįģÆč§░▒č§╗»Ę┤æ¬(Anammox)×ķų„ī¦Ż╗į┌┬²╦┘Ę┤æ¬ļAČ╬ųąŻ¼ü厧Ą¬Ą─║─▒M╩╣AnammoxĘ┤æ¬Ą─░l╔·╚▒╔┘└ĒšōŚl╝■Ż¼Č°ī”ššĮM║═╔·╬’╠┐ĮMųą╩ŻėÓ░▒Ą¬ęį╝░└█ĘeĄ─Ž§Ą¬Š∙░l╔·┴╦ŠÅ┬²Ą─Ž┬ĮĄŻ¼▀@╩Ūį┤ė┌Ę┤款wŽĄųą░l╔·┴╦▓┐ĘųĘ┤Ž§╗»ū„ė├(partialdenitrificationŻ¼PD)Ż¼įō▀^│╠─▄═©▀^īó┐ņ╦┘ļAČ╬ųą└█ĘeĄ─Ž§Ą¬▀ĆįŁ│╔ü厧Ą¬Č°╩╣Anammoxį┌┬²╦┘ļAČ╬└^└m▀MąąĘ┤æ¬ĪŻ
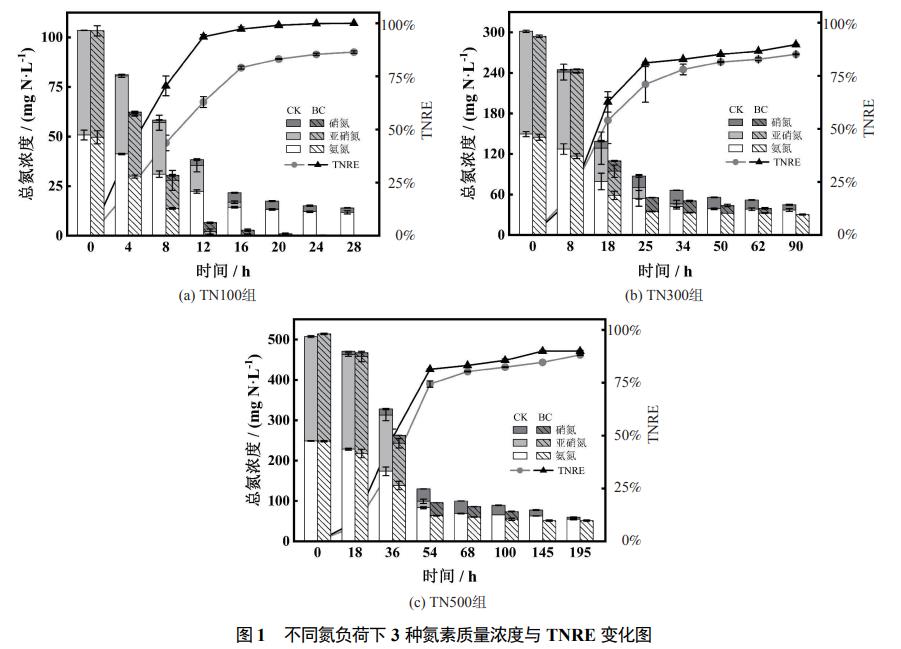
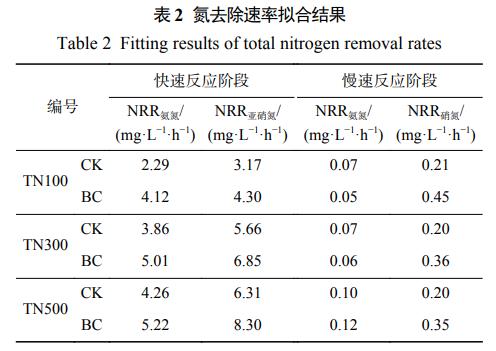
Ę┤æ¬ĮY╩°Ģr3ĮMī”ššĮMĄ─░▒Ą¬Ęųäe╩ŻėÓ11.8Īó37.1Īó54.9mgĪżL−1Ż¼Č°ī”æ¬╔·╬’╠┐ĮMĄ─░▒Ą¬Ęųäe▒╚ī”ššĮMČÓĮĄĮŌ┴╦11.8Īó6.7Īó3.5mgĪżL−1Ż╗═¼ĢrĖ∙ō■╦┘┬╩öM║ŽĮY╣¹(▒Ē2)’@╩ŠŻ¼TN100ĪóTN300ĪóTN500╔·╬’╠┐ĮMĄ─Ž§Ą¬▀ĆįŁ╦┘┬╩Ęųäe▒╚ŽÓæ¬ī”ššĮMĖ▀2.1Īó1.8Īó1.4▒ČŻ¼šf├„╔·╬’╠┐Ą─═Č╝ė═©▀^┤┘▀MŽ§Ą¬▀ĆįŁÅŖ╗»┴╦PD▀^│╠Ż¼Å─Č°▀Mę╗▓Į╠ßĖ▀┴╦AnammoxĘ┤款wŽĄĄ─┐饬╚ź│²ą¦╣¹Ż¼Ą½╔·╬’╠┐Ą─į÷ą¦ū„ė├į┌Ą═žō║╔Śl╝■Ž┬Ė³╝ė’@ų°ĪŻ▀@ę▓┼cĖ„žō║╔Ž┬Ę┤款wŽĄÜŌ¾w«a┴┐į÷╝ėĄ─┤┘▀Mą¦╣¹ŽÓę╗ų┬Ż¼TN100ĪóTN300ęį╝░TN500╔·╬’╠┐ĮMÜŌ¾w«a┴┐ĘųäeĖ▀ė┌ī”ššĮM12.9%Īó7.1%ęį╝░4.2%Ż¼│╩¼F▀f£p┌ģä▌ĪŻ
2.2 ╔·╬’╠┐į┌▓╗═¼Ą¬žō║╔Ž┬ÅŖ╗»├ōĄ¬ą¦─▄ÖC└Ē
1)╔·╬’╠┐ÅŖ╗»░¹═ŌļŖūėé„▀fī”├ōĄ¬▀^│╠Ą─ė░ĒæĪŻ
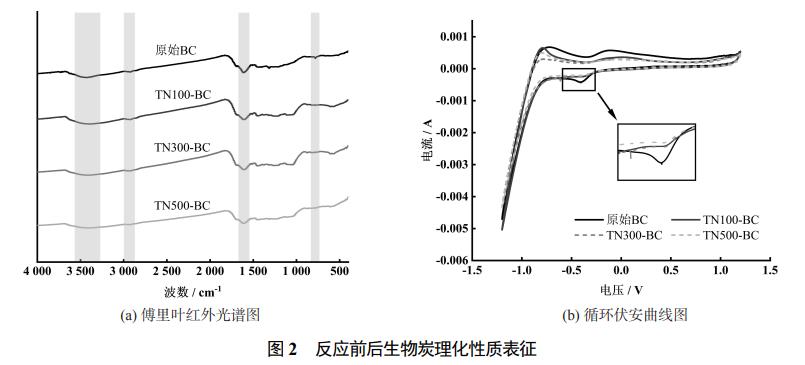
═©▀^ĖĄ└’╚~╝t═Ō╣ŌūVĘų╬÷üĒ▒Ēš„įŁ╩╝╔·╬’╠┐ęį╝░3ĘNĄ¬žō║╔Ž┬Ę┤æ¬ĮY╩°║¾╔·╬’╠┐▒Ē├µ╣┘─▄łFĄ─ūā╗»ĪŻĮY╣¹╚ńłD2(a)╦∙╩ŠŻ¼Ę┤æ¬║¾Ą─╔·╬’╠┐▒Ē├µėą▌^ČÓŠ▀ėą▀ĆįŁąįĄ─║¼č§╣®ļŖūė╣┘─▄łFŻ¼ļSų°Ą¬žō║╔Ą─╔²Ė▀Ųõ╬³╩šĘÕŠ∙ėą▓╗═¼│╠Č╚Ą─£p╚§Ż¼ŲõųąŻ¼Ęė┴u╗∙(d:3410cm−1Ż¼-OH)ęį╝░§½ŅÉ╗∙łF(b:1610cm−1)ė╚×ķ├„’@ĪŻō■蹊┐Ż¼╔·╬’╠┐▒Ē├µ┤µį┌Ą─Ęė┴u╗∙Š▀ėą▌^ÅŖĄ─╣®ļŖūė─▄┴”Ż╗§½ŅÉ╣┘─▄łF┐╔│õ«ö╝ÜŠ·Ą─░¹═ŌļŖūė╩▄¾wŻ¼═©▀^┐╔─µĄ─č§╗»▀ĆįŁčŁŁhū„ė├┤┘▀M¾wŽĄųąŽ§Ą¬Ą─▀ĆįŁŻ╗═¼ĢrĘ╝ŽŃ¤N╗∙łF(a:800cm−1Ż¼c:2880cm−1Ż¼-CH)ę▓─▄═©▀^Š▀ļŖ╗ŅąįĄ─╣▓▌m”ąļŖūėŽĄĮy┤┘▀MŽ§Ą¬▀ĆįŁ▀^│╠Ż¼╔·╬’╠┐Ą─Ę╝ŽŃąįįĮÅŖŻ¼ŲõļŖ╗ŅąįįĮÅŖŻ¼┼c▒Ē├µ╣┘─▄łFĄ─č§╗»▀ĆįŁĄ├╩¦ļŖūė▀^│╠▓╗═¼Ż¼▀@ĘNļŖūė▐DęŲ▀^│╠▓╗ąĶę¬╗»īWĘ┤æ¬Ż¼ļŖūėé„▀f╦┘Č╚Ė³┐ņĪŻę“┤╦ė╔╔Ž╩÷╣┘─▄łF╬³╩šĘÕĄ─£p╚§┌ģä▌┐╔ų¬Ż║Ę┤款wŽĄųąĄ¬žō║╔Ą─╠ßĖ▀ęŌ╬Čų°Ė³ČÓĄ─╣┘─▄łFąĶŪ¾Ż¼ė╔ė┌╔·╬’╠┐▒Ē├µ╣┘─▄łFĄ─öĄ┴┐┼c╣®ļŖūė─▄┴”ėąŽ▐Ż¼ę“┤╦╔·╬’╠┐ī”Ą═Ą¬žō║╔Ž┬Ą─AnammoxĘ┤款wŽĄ┐饬╚ź│²Š▀ėąĖ³’@ų°Ą─┤┘▀Mą¦╣¹ĪŻĖ∙ō■įŁ╩╝╔·╬’╠┐║═▓╗═¼Ą¬žō║╔Ę┤æ¬║¾╔·╬’╠┐Ą─裣hĘ³░▓Ū·ŠĆłD’@╩Š(łD2(b))Ż¼įŁ╩╝╔·╬’╠┐Ū·ŠĆ▄ē█Eųą│÷¼F┴╦ę╗ī”▓╗┐╔─µĄ─č§╗»ĘÕ┼c▀ĆįŁĘÕŻ¼Š▀ėąę╗Č©Ą─č§╗»▀ĆįŁ─▄┴”ĪŻČ°▓╗═¼žō║╔Ę┤æ¬║¾╔·╬’╠┐Ą─Ū·ŠĆłDųą▀ĆįŁĘÕŠ∙ėąę╗ų┬│╠Č╚Ą─£p╚§Ż¼┼c▓┐Ęų▀ĆįŁąį╣┘─▄łFĄ─£p╔┘┌ģä▌ę╗ų┬Ż¼šf├„įŁ╩╝╔·╬’╠┐Ą─▀ĆįŁąį─▄į┌▓╗═¼Ą¬žō║╔Ę┤款wŽĄųąŠ∙▒╗Ž¹║─Ż¼Č°ė╔ė┌Ą¬žō║╔Ą─ųØu╠ßĖ▀Ż¼╔·╬’╠┐ī”Ą═Ą¬ØŌČ╚Ą─Ę┤款wŽĄŠ▀ėąĖ³║├Ą─┤┘▀Mą¦╣¹ĪŻ
2)╔·╬’╠┐ī”EPSĮMĘų╝░┘|┴┐ØŌČ╚Ą─ė░ĒæĪŻ
īóĖ„ī”ššĮM┼c╔·╬’╠┐ĮMė┌┐ņ╦┘Ę┤æ¬ļAČ╬Īó┬²╦┘Ę┤æ¬ļAČ╬ĮY╩°ĢrĘų┼·▓Ų┐(TN100Ż║12hĪó28hŻ╗TN300Ż║25hĪó90hŻ╗TN500Ż║54hĪó195h)Ż¼╠ß╚ĪEPS▀MąąŽÓĻPųĖś╦£yČ©ĪŻEPS┼cAnAOBĄ─┤·ųx║═╗Ņąį├▄ŪąŽÓĻPŪę░lō]ų°ųžę¬ū„ė├Ż¼ų„ę¬ė╔PS║═PNĮM│╔ĪŻė╔łD3(a)┐╔ų¬Ż¼Ę┤æ¬Ų┌ķg╔·╬’╠┐ĮMĄ─EPS(PN+PS)║¼┴┐╗∙▒ŠĖ▀ė┌ī”ššĮMŻ¼ŪęĖ„įć“×ĮMĄ─EPS┘|┴┐ØŌČ╚Š∙ļSų°Ą¬žō║╔Ą─╠ßĖ▀Č°Ž┬ĮĄŻ¼▀@┼cYANGĄ╚Ą─蹊┐ĮY╣¹ę╗ų┬┐╔─▄į┤ė┌EPSųąĄ─▓┐ĘųėąÖC│╔Ęųģó┼cŽ§Ą¬▀ĆįŁĄ─ūįBĘ┤æ¬Č°▒╗Ž¹║─ĪŻ┬²╦┘ļAČ╬Ą─ŲĮŠ∙EPS┘|┴┐ØŌČ╚Š∙Ą═ė┌┐ņ╦┘ļAČ╬Ż¼▀@╩Ūė╔ė┌Ė³Ė▀Ą¬žō║╔¾wŽĄĢ■«a╔·Ė³Ė▀Ą─└█ĘeŽ§Ą¬┐é┴┐Ż¼Č°EPSį┌¤o═Ō╝ė╠╝į┤Ą─ūįB¾wŽĄųą│õ«ö╬©ę╗Ą─ėąÖC╠╝į┤Ż¼ę“┤╦į┌ģó┼cŽ§Ą¬▀ĆįŁĄ─▀^│╠ųąŽ¹║─┴┐ųØuį÷┤¾ĪŻTN100ĮM╔·╬’╠┐ī”EPSØŌČ╚Ą─╠ß╔²ą¦╣¹ūŅ╝čŻ¼Ūę╠ß╔²ą¦╣¹ļSų°žō║╔Ą─į÷╝ėČ°Ž┬ĮĄŻ¼▀@┼c╔·╬’╠┐┤┘▀MŽ§Ą¬▀ĆįŁ╦┘┬╩╠ßĖ▀Ą─┌ģä▌ę╗ų┬Ż¼┐╔─▄╩Ūę“×ķ╔·╬’╠┐═©▀^Ųõč§╗»▀ĆįŁ╗Ņąį┼c╣®ļŖūė─▄┴”┤┘▀M┴╦Ž§Ą¬▀ĆįŁ▀^│╠Ż¼Å─Č°ÅŖ╗»╝ÜŠ·┤·ųx┼cEPSĄ─Ęų├┌ĪŻ
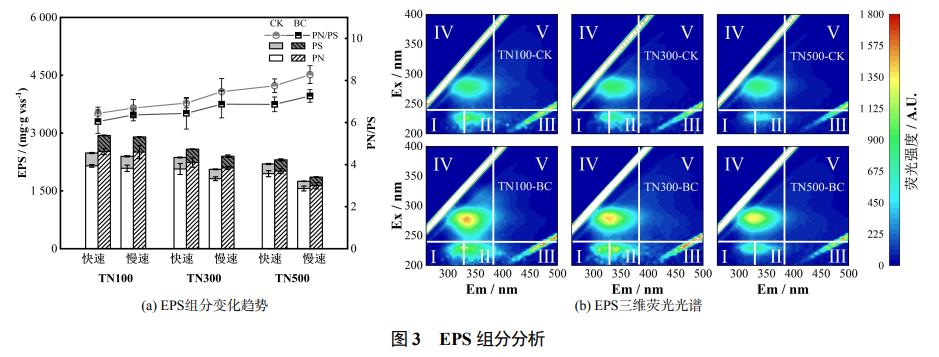
EPSĮMĘųĘų╬÷’@╩ŠŻ¼PN╩ŪEPSĄ─ų„ę¬ĮM│╔▓┐ĘųŻ¼Ųõį┌Ė„īŹ“×ĮMEPS║¼┴┐ųą▒╚└²│¼▀^80%Ż¼▀@┐╔─▄į┤ūįė┌EPSį┌╬ó╔·╬’║═Ąū╬’ų«ķgū„×ķļxūė▀\▌ö═©Ą└Ą──▄┴”ęį╝░ūį╔Ēģó┼c┤╦ŅÉų„äė▀\▌öĄ─ĮY╣¹ĪŻėąčąŠ┐▒Ē├„Ż¼PN/PS╩Ū▒Ē╩ŠŅw┴Ż╬█─ÓĘĆČ©ąįĄ─ųĖś╦Ż¼▌^Ė▀Ą─PN/PS▒╚╚▌ęūī¦ų┬AnammoxŅw┴Ż╬█─ÓĄ─ÅŖČ╚ĮĄĄ═║═│┴ĮĄ─▄┴”Ž┬ĮĄŻ¼Č°TN100ī”ššĮM┼c╔·╬’╠┐ĮMŲĮŠ∙PN/PSųĄ×ķ6.6Īó6.2Ż¼Ą═ė┌TN500Ą─8.0Īó7.1ĪŻŠC╔Ž╦∙╩÷Ż¼╔·╬’╠┐į┌▌^Ą═Ą¬žō║╔Ž┬ÅŖ╗»AnammoxĘ┤款wŽĄEPSĘų├┌║¼┴┐Ė³╝ė’@ų°Ż¼═¼ĢrŠ▀ėąūŅĄ═Ą─PN/PS▒╚Ż¼šf├„╔·╬’╠┐Ą─═Č╝ė╠ßĖ▀┴╦╬ó╔·╬’łFŠ█║═ĘĆČ©ąįŻ¼Å─Č°īŹ¼FĄ═Ą¬žō║╔Ž┬╔·╬’╠┐ĮMĖ³║├Ą─├ōĄ¬ąį─▄ĪŻ
łD3(b)š╣╩Š┴╦Ę┤æ¬ĮY╩°║¾Ė„žō║╔Ž┬ī”ššĮM┼c╔·╬’╠┐ĮMĄ─╚²ŠS¤╔╣Ō╣ŌūV╠žąįĪŻEPSųąĖ„ĘNĄ░░ū┘|╬’┘|┐╔Ė∙ō■▓╗═¼╠žąįĘų×ķ5éĆģ^ė“Ż║Ę╝ŽŃŅÉĄ░░ū┘|ó±(ó±)ĪóĘ╝ŽŃŅÉĄ░░ū┘|ó“(ó“)Ż╗Ė╗└’╦ß(ó¾)Ż╗┐╔╚▄ąį╬ó╔·╬’«a╬’(IV)Ż╗Ė»ų▓╦ß(V)ĪŻį┌Ė„ĮM¤╔╣ŌłDūVųą┐é╣▓┤_Č©┴╦3éĆų„ę¬ĘÕŻ║Ex/Em=(235~240)nm/(325~330)nmĪóEx/Em=(235~240)nm/(345~345)nmęį╝░Ex/Em=(275~280)nm/(335~340)nmŻ¼╝┤Ę╝ŽŃŅÉĄ░░ū┘|ó±(ó±)ĪóĘ╝ŽŃŅÉĄ░░ū┘|ó“(ó“)║═┐╔╚▄ąį╬ó╔·╬’«a╬’(ó¶)ĪŻ┐╔ęį░l¼FĖ„╔·╬’╠┐ĮMųą▀@ą®ĘÕĄ─¤╔╣Ōģ^Š∙Ė▀ė┌ŽÓæ¬ī”ššĮMŻ¼Ųõųąį÷╝ėūŅ├„’@Ą─ģ^ė“×ķ┐╔╚▄ąį╬ó╔·╬’«a╬’Ż¼ŪęŲõ¤╔╣Ōģ^ÅŖČ╚┼c├µĘeĄ─į÷╝ė│╠Č╚ļSų°Ą¬žō║╔Ą─╠ßĖ▀Č°£p╔┘ĪŻčąŠ┐▒Ē├„EPSųąĄ─┐╔╚▄ąį╬ó╔·╬’«a╬’Ą─║¼┴┐╦«ŲĮ┐╔Ę┤ė│ģÆč§╬ó╔·╬’Ą─╗ŅąįŻ¼Č°╔·╬’╠┐╠ß╔²▓╗═¼Ą¬žō║╔Ę┤款wŽĄ├ōĄ¬ą¦╣¹Ą─┌ģä▌┼cEPSųą┐╔╚▄ąį╬ó╔·╬’«a╬’Ą─£p╔┘┌ģä▌ę╗ų┬Ż¼šf├„Ą═žō║╔Ę┤款wŽĄŠ▀ėąĖ³ÅŖĄ─╬ó╔·╬’╗ŅąįŻ¼Å─Č°┤┘▀M┴╦Ą═Ą¬žō║╔Śl╝■Ž┬┐饬╚ź│²ą¦╣¹Ą─╠ß╔²ĪŻ
2.3 ╬ó╔·╬’╚║┬õč▌╠µ╠žš„╝░┤·ųxūā╗»
1)╔·╬’╠┐ī”╚║┬õĮYśŗ╝░Š█╝»╠žš„Ą─ė░ĒæĪŻ
Ė▀═©┴┐£yą“ĮY╣¹’@╩ŠŻ¼Ė„žō║╔Ž┬AnammoxĘ┤款wŽĄųąį┌ķT╦«ŲĮš╝ų„ī¦Ą─╬ó╔·╬’ų„ę¬░³└©Planctomycetes(ĖĪ├╣Š·ķT)ĪóProteobacteria(ūāą╬Š·ķT)ĪóChloroflexi(ŠG×│Š·ķT)ĪóBacteroidetes(öMŚUŠ·ķT)ĪóFirmicutes(║±▒┌Š·ķT)ĪóArmatimonadetes(čb╝ūŠ·ķT)ĪóIgnavibacteriaęį╝░unclassifiedBacteriaĪŻĘ┤Ž§╗»Š·ī┘ę╗░Ńļ`ī┘ė┌ProteobacteriaĪóFirmicutes║═BacteroidetesŻ¼ģÆč§░▒č§╗»Š·ī┘ļ`ī┘ė┌PlanctomycetesĪŻ
Ę┤款wŽĄā╚ų„ꬥ─ī┘×ķCandidatusKueneniaĪóunclassifiedBetaproteobacteriaĪóunclassifiedBacteriaĪóunclassifiedAnaerolineaceaeĄ╚Ż¼ŲõųąCandidatusKuenenia×ķAnammoxĘ┤款wŽĄųąūŅų„ꬥ─AnAOBŻ╗═¼Ģr¾wŽĄųąėąČÓĘNDNB╣▓┤µŻ¼╚ńAcinetobacterĪóAfipiaĪóIgnavibacteriumĪóPseudomonasĪóChryseobacteriumĄ╚ĪŻ╔·╬’╠┐Ą─═Č╝ė╠ßĖ▀┴╦AnAOBĄ─žSČ╚Ż¼╠ß╔²ą¦╣¹ūŅ╝č×ķTN100╔·╬’╠┐ĮMŻ¼ŽÓ▌^ė┌ī”ššĮM╠ßĖ▀┴╦11.0%Ż¼TN300╔·╬’╠┐ĮM║═TN500╔·╬’╠┐ĮMĘųäe╠ßĖ▀┴╦7.4%┼c4.4%(łD4(a))Ż╗Ųõ┤╬Ż¼╔·╬’╠┐ę▓┤┘▀M┴╦Acinetobacter║═Afipia▀@2ĘNā×ä▌DNBžSČ╚Ą─╠ßĖ▀Ż¼ŪęTN100╔·╬’╠┐ĮM┐éĘ┤Ž§╗»Š·ī┘žSČ╚╠ß╔²│╠Č╚ūŅĖ▀×ķ8.4%Ż¼┼cTN100╔·╬’╠┐ĮMŠ▀ėąūŅā×┐饬╚ź│²ą¦╣¹ī”æ¬ĪŻ┤╦═ŌŻ¼Armatimonadetesgp5Š▀ėąĮĄĮŌČÓ╠ŪĄ──▄┴”Ż¼ŲõžSČ╚ļSĄ¬ØŌČ╚Ą─į÷╝ėČ°╠ßĖ▀Ż¼Ę¹║ŽEPSĮMĘųųąČÓ╠ŪĄ─ĮĄĮŌ┌ģä▌ĪŻ
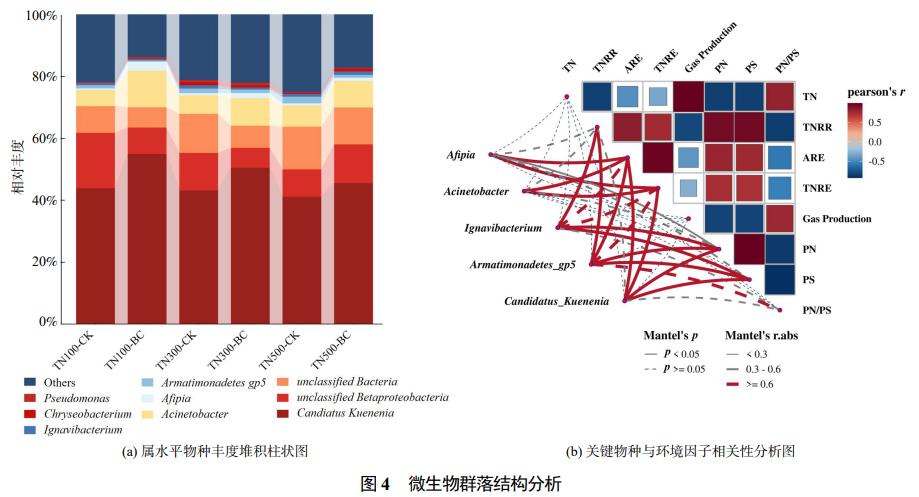
╗∙ė┌蹊┐ĮY╣¹▀Mąą┴╦MantelÖz“ׯ¼Ęų╬÷┴╦ĻPµIŠ·ī┘┼c▓╗═¼ŁhŠ│ę“ūėų«ķgĄ─ŽÓĻPąį(łD4(b))ĪŻĮY╣¹’@╩ŠŻ¼ĻPµIAnAOB║═DNBĄ─žSČ╚┼cTNREŠ▀ėąŽÓĻPąįŻ¼╚ńCandidatusKuenenia(Ż³rŻ³=0.67Ż¼p<0.05)ĪóAcinetobacter(Ż³rŻ³=0.73Ż¼p<0.01)Ż¼×ķ╠ß╔²TNREĄ─ų„ę¬ū„ė├Š·╚║ĪŻČ°Ignavibacterium┼cPNĪóPS┘|┴┐ØŌČ╚Š▀ėąŽÓĻPąį(Ż³rŻ³=0.86Ż¼p<0.05Ż¼PNŻ╗Ż³rŻ³=0.82Ż¼p<0.05Ż¼PS)Ż¼šf├„Ignavibacterium┐╔─▄į┌EPSĄ─Ž¹║─▀^│╠ųą░lō]ųžę¬ū„ė├ĪŻŲõ┤╬Ż¼PearsonŽÓĻPąįĘų╬÷’@╩ŠŻ¼TN┼cPN/PS│╩š²ŽÓĻP(r=0.82)Ż¼šf├„Ą¬žō║╔Ą─╠ßĖ▀ė░Ēæ┴╦EPSĄ─ĮM│╔Ż╗TNRR┼cPNĪóPS│╩š²ŽÓĻP(r=0.94Īór=0.95)Ż¼¾w¼F│÷├ōĄ¬╦┘┬╩Ė▀Ą─Ę┤款wŽĄŠ▀ėąĖ³Ė▀Ą─EPSĘų├┌╦«ŲĮĪŻ
Ė∙ō■Æ▀├ĶļŖńRłD(łD5Ż®’@╩ŠŻ¼į┌▓╗═¼Ą¬žō║╔Śl╝■Ž┬Ż¼╬ó╔·╬’Š█╝»ŪķørŠ▀ėąę╗Č©▓Ņ«ÉĪŻĖ∙ō■ĘNūėŅw┴Ż╬█─Ó▒Ē├µŠ·╚║ą╬æB(łD5dŻ®┐╔ų¬╬ó╔·╬’Ą─ų„ꬹ╬æB×ķŪ“ĀŅŻ¼┼cĖ„Ą¬žō║╔Ę┤款wŽĄųą╔·╬’╠┐▒Ē├µĖ╗╝»Ą─╝ÜŠ·ą╬æBę╗ų┬ĪŻį┌3ĘNAnammoxĘ┤款wŽĄųąŻ¼ė╔ė┌TN500╔·╬’╠┐ĮMĄ¬žō║╔ūŅĖ▀Å─Č°Š▀ėąĖ³ķLĄ─Ę┤æ¬ĢrķgŻ¼╔·╬’╠┐╔Ž╬ó╔·╬’Ą─Š█╝»Ė³╝ė’@ų°Ż¼ęįČÓéĆŅw┴ŻŠ█╝»¾wĄ─ą╬æBżĖĮį┌╔·╬’╠┐▒Ē├µĪŻČ°į┌Ą═Ą¬žō║╔Ę┤款wŽĄĄ─TN100╔·╬’╠┐ĮMųąŻ¼Ę┤æ¬║¾╔·╬’╠┐▒Ē├µ╬ó╔·╬’Ė╗╝»│╠Č╚▌^Ą═Ż¼šf├„į┌Ė▀žō║╔Ę┤款wŽĄųąĖ▀ØŌČ╚Ą¬╦žĄ─ęųųŲū„ė├ė░Ēæ╬ó╔·╬’ĢrŻ¼╔·╬’╠┐═©▀^×ķ╝ÜŠ·╠ß╣®Ė╗╝»╬╗³cīŹ¼FĖ³ķLĢrŲ┌Ž┬┐饬Ą─ĘĆČ©╚ź│²ĪŻ

2)╔·╬’╠┐ÅŖ╗»┤·ųxĪŻ
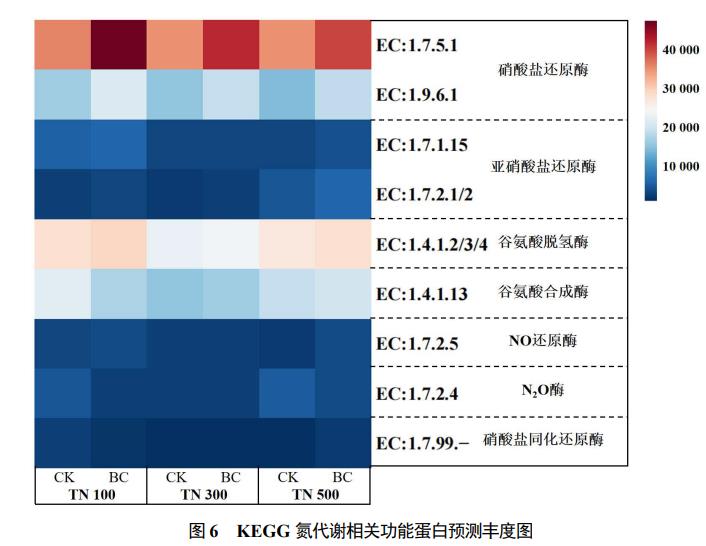
Ė∙ō■KEGGöĄō■Äņ▒╚ī”ĮY╣¹▀x╚ĪĄ¬┤·ųx═©┬Ę(M00910)▀MąąĘų╬÷Ż¼ę╗╣▓½@Ą├38Śl╚²╝ē┤·ųx═ŠÅĮŻ¼▀x╚ĪŲõųą18ŚlŽÓĻP═©┬Ę▓ó░┤▓╗═¼╣”─▄Ą░░ūĘų│╔7ŅÉĪŻ╚ńłD6╦∙╩ŠŻ¼╔·╬’╠┐ĮMųąė╔ECŻ║1.7.5.1ĪóECŻ║1.9.6.1śŗ│╔Ą─Ž§╦ß¹}▀ĆįŁ├ĖĄ─žSČ╚ėą’@ų°Ą─į÷╝ėŻ¼ŪęļSų°Ą¬žō║╔ĮĄĄ═Č°╠ßĖ▀Ż¼šf├„Ą═žō║╔Ę┤款wŽĄ(TN100)Š▀ėąĖ³Ė▀Ą─Ž§Ą¬▀ĆįŁÅŖČ╚Ż╗╔·╬’╠┐Ą─═Č╝ėį÷╝ė┴╦╣╚░▒╦ß├ōÜõ├Ė(ECŻ║1.4.1.2/3/4)┼c╣╚░▒╦ß║Ž│╔├Ė(ECŻ║1.4.1.13)Ą─žSČ╚Ż¼¾w¼F│÷╔·╬’╠┐į÷ÅŖ┴╦AnammoxĘ┤款wŽĄĄ─╝Ü░¹┤·ųx╗ŅąįŻ¼Č°TN100╔·╬’╠┐ĮMŽÓĻP╣”─▄Ą░░ūžSČ╚ūŅĖ▀Ż¼Å─Č°īŹ¼F┴╦╔·╬’╠┐┤┘▀MĄ═Ą¬žō║╔Ž┬Ę┤款wŽĄ┐饬╚ź│²┬╩╠ß╔²Ė³Ė▀Ą─ĮY╣¹ĪŻ
3ĪóĮYšō
1)▓╗═¼Ą¬žō║╔Ž┬╔·╬’╠┐ī”ģÆč§░▒č§╗»┐饬╚ź│²Ą─╠ß╔²ą¦╣¹×ķTN100>TN300>TN500Ż¼ŪęŽÓī”ė┌ī”ššĮMĘųäe╠ß╔²┴╦13.6%Īó4.5%Īó1.8%Ż¼═¼ĢrTN100╔·╬’╠┐ĮMŠ▀ėąūŅĖ▀Ą─┐饬╚ź│²╦┘┬╩(0.103gNĪżL−1Īżd−1)ęį╝░ūŅĖ▀Ą─┐饬╚ź│²ą¦┬╩(100%)Ż¼šf├„Ą═Ą¬žō║╔Śl╝■Ž┬╔·╬’╠┐ī”ģÆč§░▒č§╗»¾wŽĄ┐饬╚ź│²Ą─┤┘▀Mą¦╣¹Ė³╝čŻ¼▀@╩Ūę“×ķĄ═Ą¬žō║╔Ę┤款wŽĄųą╔·╬’╠┐┤┘▀MPD▀^│╠Ė³╝ė’@ų°Ż¼īŹ¼F┴╦╩ŻėÓ░▒Ą¬┼c└█ĘeŽ§Ą¬Ą─╔ŅČ╚╚ź│²ĪŻ
2)╔·╬’╠┐▒Ē├µ║¼č§╣┘─▄łF╠ß╣®Ą─ļŖūėĪó╔·╬’╠┐▒Š╔ĒĄ─č§╗»▀ĆįŁ─▄┴”ęį╝░┤┘▀M╬ó╔·╬’EPSĘų├┌╩ŪÅŖ╗»Ž§Ą¬▀ĆįŁ▀^│╠Ą─ĻPµIę“╦žŻ¼┐饬╚ź│²ą¦┬╩ūŅĖ▀Ą─TN100╔·╬’╠┐ĮMŠ▀ėąĖ³Ė▀Ą─EPSŲĮŠ∙┘|┴┐ØŌČ╚ęį╝░Ė³Ą═Ą─PN/PSĪŻ
3)╔·╬’╠┐Ą─═Č╝ė╠ß╔²┴╦Ę┤款wŽĄųąų„ę¬AnAOBŻ║CandidatusKuenenia┼cų„ę¬DNBŻ║Acinetobacter║═AfipiaĄ─žSČ╚Ż¼═¼Ģr╔·╬’╠┐į÷ÅŖ┴╦Ž§╦ß¹}▀ĆįŁ├ĖŽÓĻP╣”─▄Ą░░ūĄ─╗ŅąįŻ¼ŲõųąTN100╔·╬’╠┐ĮMŠ▀ėąūŅĖ▀žSČ╚Ż¼īŹ¼F┴╦╔·╬’╠┐┤┘▀MĄ═Ą¬žō║╔Ž┬Ę┤款wŽĄ┐饬╚ź│²┬╩╠ß╔²Ė³’@ų°Ą─ĮY╣¹ĪŻŻ©üĒį┤Ż║╬„░▓Į©ų■┐Ų╝╝┤¾īWŁhŠ│┼c╩ąš■╣ż│╠īWį║Ż¼¢|▒▒┤¾īW╣ż│╠蹊┐╔·į║═┴─Š┼cŁhŠ│╣ż│╠ŽĄŻ®



